
据NDT中文版微信公众平台2019年9月16日讯 在透析治疗终末期肾病(ESRD)的早期,即发现并非与ESRD相关的所有发病均可归因于小分子水溶性物质(如尿素)的潴留。在20世纪80年代中后期,确定了11.8kDaβ2-微球蛋白,是长期血液透析患者严重关节病相关淀粉样沉积物的主要成分,这是较高分子量尿毒素存在的确凿证据,由此激发了对去除此类毒素的膜的新兴趣。
随后,随着分析生物化学的进展,使人们能够鉴别出分子量高达40kDa的种类繁多的中分子,其中许多中分子与尿毒症毒性的不同方面有关。随着大小约为60kDa溶质的存在和毒性证据不断积累,越来越清楚的是,亟需新策略及性能特征与自体肾脏更接近的膜将这类毒素清除。
本文总结了目前透析膜的性能,并说明了最新膜技术进展如何使溶质清除特性更接近自体肾。
透析膜的性能特征
目前的透析膜根据β2-微球蛋白清除率和筛选系数,常规被分成两大类,即低通量膜和高通量膜(表)。如超滤系数所示,水渗透性在过去的一些分类中使用过,但已不再是临床相关的性能指标,因为使用所有高通量膜都需要能够控制超滤的透析机。这种简单的将膜分类为低通量或高通量的方法现在正受到挑战,因为开发了新的渗透性更强的膜,这些膜被不同地描述为中截留量、蛋白渗漏、高截留量和其他定义不太明确的术语,如超通量和超高通量。这些新膜将如何分类仍有待确定。
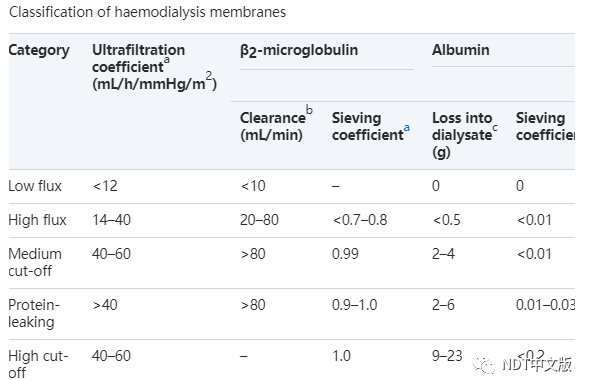
a.体外。b.用于血液流速为300~400mL/min的传统血液透析,包括扩散、对流和吸附作用。c.用于4h常规血液透析。
初步观察性研究表明,使用高通量膜与发病率和死亡率改善相关,随后进行了两项大型RCT,血液透析(HEMO)研究和膜渗透性结局(MPO)研究。除患者亚组的事后分析外,两项研究均未显示高通量膜的显著生存获益。
在HEMO和MPO研究之后,推测血液透析通过高通量膜清除中分子尿毒素不足以获得生存获益。血液透析的溶质清除主要通过扩散进行,随着分子大小的增加,扩散迅速下降。相比之下,对流对溶质大小的增加不太敏感。因此,引入的结合弥散和对流的血液透析滤过(HDF)是增加中分子溶质清除的一种方式,这超出了高通量血液透析的可能。
有三项RCT,旨在检验在线后稀释HDF与低通量或高通量血液透析相比改善ESRD患者全因死亡率的能力。这3项研究的结果不一,仅1项研究表明接受HDF治疗患者的全因和感染相关死亡风险显著低于接受高通量HD治疗的患者。然而,研究结果的解释是复杂的,对3项RCT汇总的个体患者数据进行二次分析,再加上第4项研究,发现HDF与对流体积最高三分位数患者的死亡相对风险显著降低相关。总之,RCT的结果支持使用高对流容量时,HDF提供的中分子尿毒素的卓越清除在改善患者生存率起了作用。
虽然使用具有高对流体积的在线HDF来增加中分子尿毒素的清除似乎是有益的,但也有其不利因素。进行HDF需要专门且昂贵的设备,如果增加总透析液流速以维持通过透析器的透析液流量和小溶质的扩散清除,则透析液(水和浓缩液)消耗可能增加高达40%,并且存在与在线制备和输注大量无菌无致热原置换液相关的潜在风险。开发渗透性相对分子大小特征更接近天然肾脏的新型膜用于血液透析,在在线HDF中不增加外部对流,将是解决这些潜在不利的一种方法。
开发更接近模拟天然肾脏的膜所面临的挑战
制造更接近模拟天然肾脏的渗透性特征的膜的除相关科学之外,挑战在于不增加有益蛋白质损失。血清白蛋白浓度取决于其合成和分解代谢速率、其在身体各室之间的分布和外部损失(如进入透析液)。
炎症与白蛋白合成减少相关。在ESRD患者中,炎症可导致血清白蛋白浓度稳定下降。因此,在评估血清白蛋白浓度的任何变化并发生在膜允许白蛋白进入透析液而丢失增加的情况时,应考虑是否存在炎症。传统血透进入透析液的白蛋白很少。最常用的透析器报告的每次治疗的白蛋白损失量范围为0.5~4.2g,后稀释HDF则损失更大。使用可比透析器已进行了4项比较HDF与传统血液透析的RCT。在这些研究中,HDF治疗组的血清白蛋白浓度无差异或仅略低于常规血液透析治疗组,表明白蛋白损失水平不会造成风险。现有数据表明,在不存在炎症的情况下,使用的透析器损失≤12g每周对患者几乎没有风险,而日常使用白蛋白损失≥20g/周的透析器膜时应相当谨慎。
透析膜分类
虽然使用β2-微球蛋白清除率和筛分系数区分低通量和高通量膜已被广泛接受,但如何对新的渗透性更强的膜进行分类尚未达成共识。由于新膜旨在用于增强中分子尿毒素的清除,因此基于这些溶质清除的分类似乎是最合适的。设想高通量膜可分为三类:(i)与目前广泛使用的膜相对应的标准高通量膜;(ii)范围扩大的膜,可通过扩散和对流结合清除比标准高通量膜更高的中分子,不依赖外部置换液,白蛋白损失临床不显著;(iii)蛋白渗漏膜,能够在不输注外部置换液的情况下清除范围扩大的较高分子量的中分子,但白蛋白损失显著。
区分三类高通量膜需要建立一些新的性能标准。β2-微球蛋白清除率可用于区分低通量膜和高通量膜,但β2-微球蛋白清除率可用于区分低通量和高通量膜,但却不适用于将标准高通量膜从扩大范围和蛋白渗漏膜中分开。
但对于从扩大范围和蛋白渗漏膜中分离标准高通量膜无效。后两类膜和标准高通量膜之间的界限可以根据其他高分子量蛋白的清除率和筛分系数来确定,如YKL-40(40kDa)或正五聚蛋白3(45kDa)。最后,透析液中的白蛋白损失可用于区分范围扩大的膜和蛋白渗漏膜。如前所述,当前数据表明,区分扩大范围膜和蛋白渗漏膜的白蛋白损失水平可设定为平均≤4g/治疗,每周3次治疗,扩大范围膜的绝对上限为6.7g/治疗。
研究者说
严格控制用于膜制造的聚合物的分子特征及添加剂,并改进生产工艺,使得膜的孔径分布更严格,允许使用增加的绝对孔径,而不会泄漏大量白蛋白。同时,膜纤维的壁厚和内径减小,增强了透析器内的对流转运,而不需要外部置换液。当用于传统血液透析时,这些新的范围扩大的膜比目前可用的膜提供了更像天然肾脏的溶质清除特性。



